I numeri quantici servono a definire la
struttura degli atomi:
livello energetico, numero e forma degli
orbitali,numero di elettroni.
I Numeri quantici (NQ) sono 4:
NQ principale : simbolo n
NQ secondario : simbolo l
NQ magnetico: simbolo: ml
NQ di spin: simbolo : ms
I NQ sono a tutti gli effetti dei
numeri che a loro volta “spiegano” o “rimandano”
cio' a cui si riferiscono cioe'
il livello energetico, il tipo di
orbitale e quindi la sua forma, l'orientamento e l'energia associata.
Un orbitale e' una zona dello spazio in
cui e' piu' probabile trovare un elettrone.
In un orbitale possono coesistere al
massimo 2 elettroni ma con un diverso (“opposto”) numero
di spin.
I NQ sono tra loro collegati a cascata
attraverso “formule”:
dal primo dipende il secondo il
secondo dal terzo, ma il quarto e' indipendente potendo avere solo
due valori.
Il numero quantico principale n,
e' un numero intero che va da 1 a 7 (anche oltre ma non ha
praticita' per la configurazione elettronica)
Il numero quantico n precisa il
livello energetico. Piu' alto e' il numero piu' elevata e' l'energia
ad esso associata.
I livelli da 1 a 7 sono indicati anche
dalla lettere che vanno da K a Q
Il numero quantico secondario l
indica i tipi (forme) di orbitali associati a quel livello e
indirettamente anche la loro grandezza. Dato che piu' alto e' n piu'
grande e' il raggio dell'atomo
I valori del NQ l dipendono dl NQ n
attraverso la seguente formula:
l = compresi tra 0 e n -1 ovvero
0 < l < n-1
quindi n = 1 , l = 0
... 0 = orbitale s
n=2 , l=
0 1 ... 1 = orbitale p
n=3 , l=
0 1 2 ... 2= orbitale d
n=4 , l=
0 1 2 3 ... 3 = orbitale f
ovvero per n=4 coesistono gli orbitali 0=s, 2=p, 3=d e infine 4=f
Riassumento:
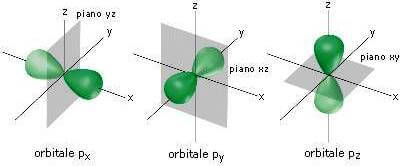
l=0 orbitale sferico
l=1 orbitale di tipo p 2 lobi
l=2 orbitale di tipo d 4 lobi
l=3 orbitale di tipo f 8 lobi
Per
l = 0 l'orbitale (s) è sferico. Al centro della sfera c'è
il nucleo.

Per
l = 1 l'orbitale ( p ) è a due lobi Il nucleo dell'atomo sta
al centro dei due lobi.

Per
l = 2 = orbitale ( d ) : è a quattro lobi . Il nucleo
dell'atomo sta al centro dei quattro lobi.

Per
l = 3 = l'orbitale f : è a otto lobi (orbitale f).

il numero quantico magnetico ml
indica quante direzioni sono possibili per ogni orbitale nello spazio e,
indirettamente il numero di orbitali
possibili
Il valore del NQ ml e' compreso tra
-l e l cioe' : - l < ml < l
n=1 ... l= 0 ... ml = 0 : Valore 0 ovvero nessuna particolare orientazione
infatti l=0 e' l'orbitale sferico e quindi i tre assi sono itercambiabili

n=2 ... l= 0, 1 ... per l=0 si ha ml=0 ; per l=1 si ha:
ml = -1 0 1
cioe' valori di tre possibili orientamenti e quindi anche 3 orbitali
n=3 l=0,1,2 ..... per l=2
.... ml= -2 -1 0 1 2
cioe' 5 possibili orientamenti e quindi 5 possibili orbitali

n=4 l=0,1,2,3
per l=3 ml= -3 -2 -1 0 1
2 3 ... ovvero in tutto 7 possibili orientamenti

il numero quantico di spin puo'
assumere due valori -1/2 e ½
Ogni elemento
della tavola periodica ha dunque una propria precisa configurazione
elettronica
dato che a parita' dei valori di n, l, ml
il valore
di spin differenzia due atomi “similari”
Il
modo pero' in cui gli orbitali vengono occupati dagli elettoni
a
partire dall’Idrogeno sino all’Uranio e oltre sino all'elemento
118
ha una successione particolare dato
che i livelli energetici degli orbitali s p d f non sono
rigidamente in scala.
Il
loro riempimento dipende
dal fatto che che alcuni
orbitali di livello più basso
sono più energetici di
altri a livello più alto
ma
in generale lo schema di
riepimento degli orbitali e' il seguente:
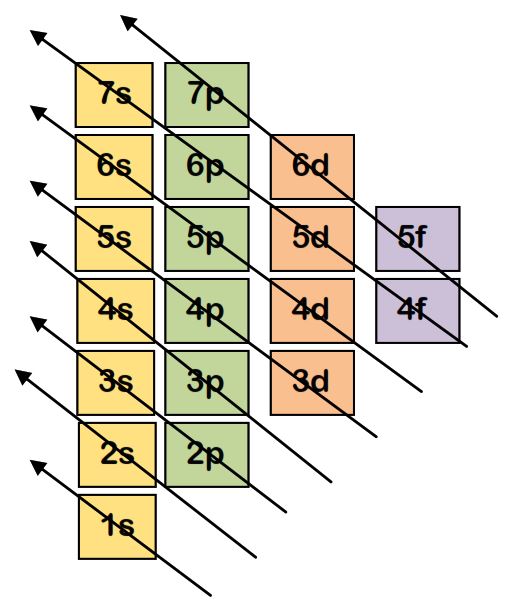
Si riempiono prima quelli intercettati
dalla stessa freccia :
ad esempio dopo il 4p viene occupato il 5s e solo
successivamente il 4d
Qusto e’ un altro schema per
illustrare la stessa cosa
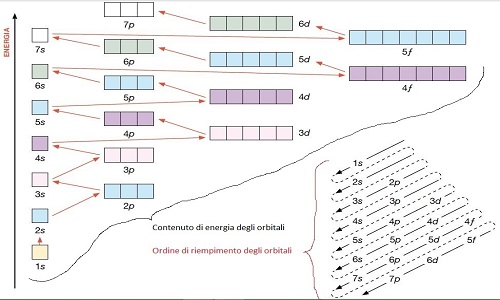
A parita di "energia" si occupano gli orbitali con un elettrone e poi si completano gli altri.
Esempio: caso degli orbitali 2p
si occupa 2px poi 2py poi 2pz e solo dopo si completa il 2px
Prima pero' di passare ad un orbitale di energia superiore si completa/no quello/i di energia inferiore.

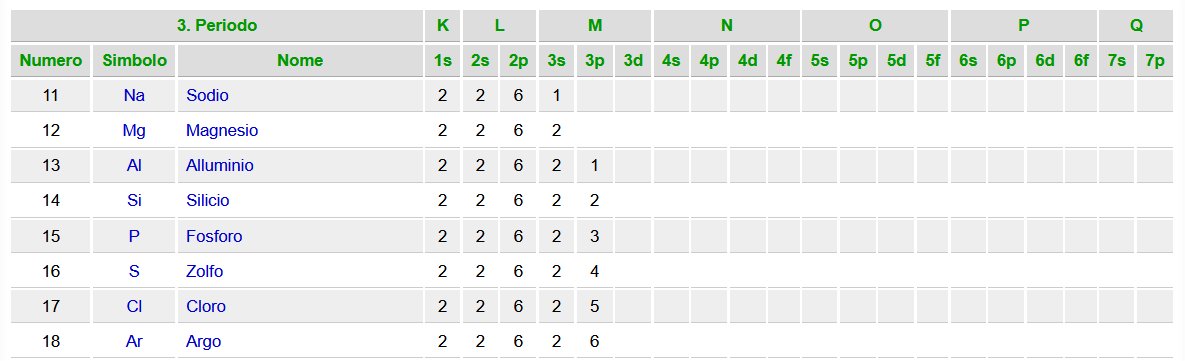
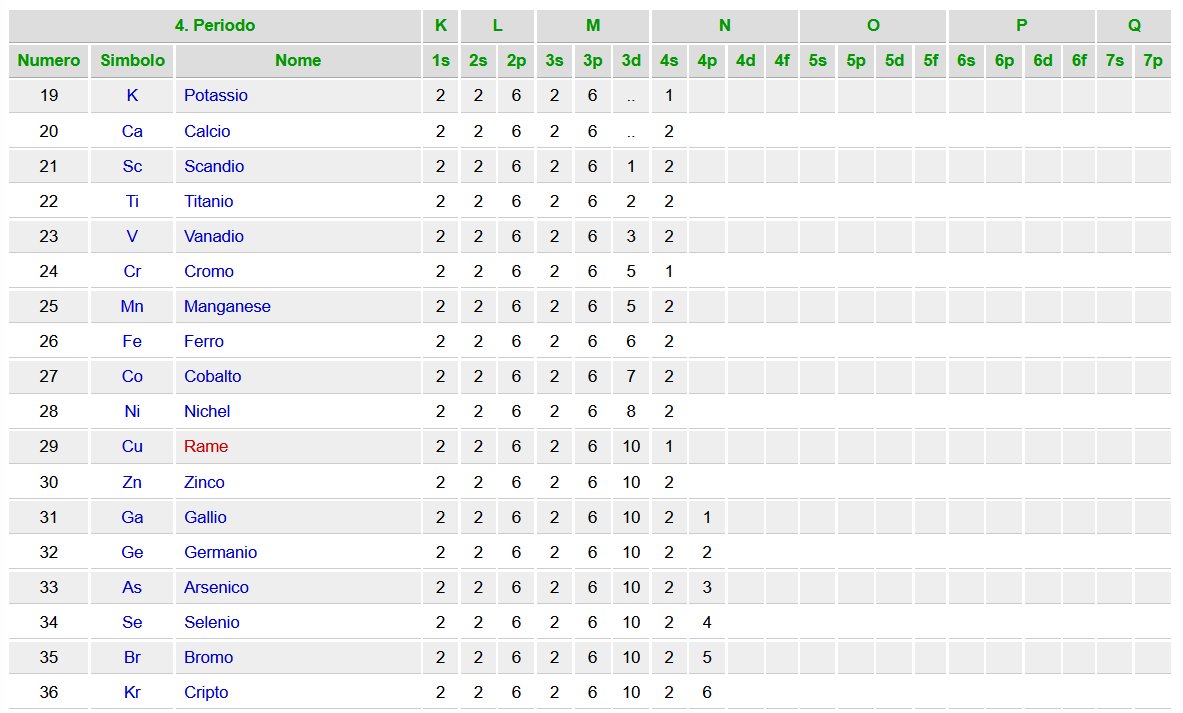
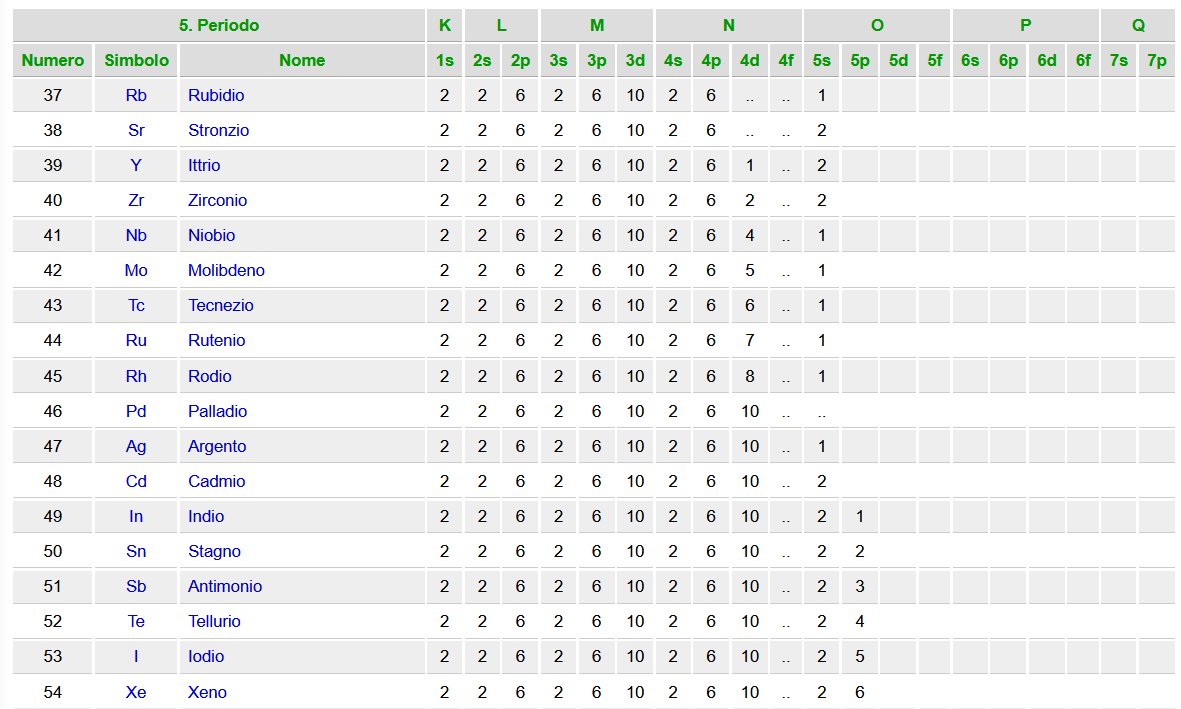
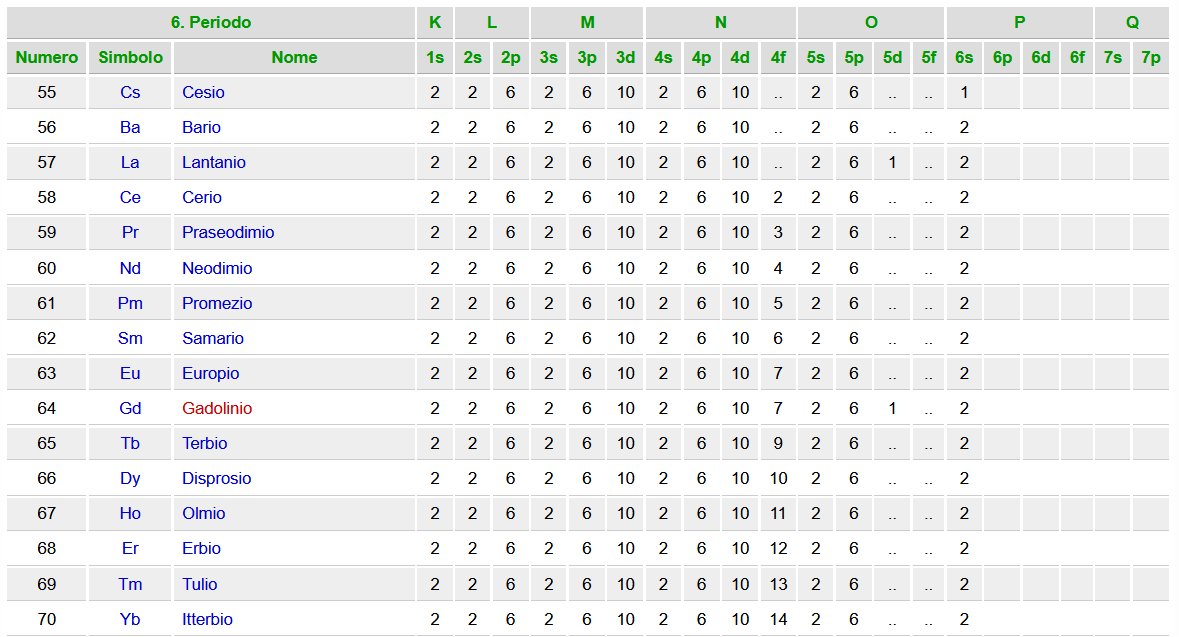

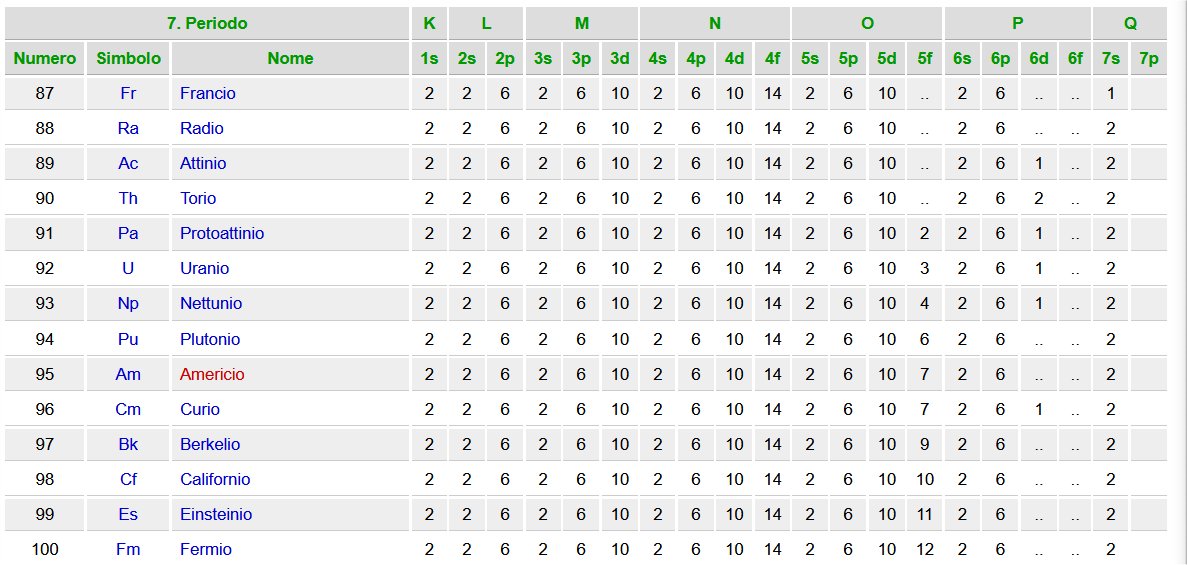

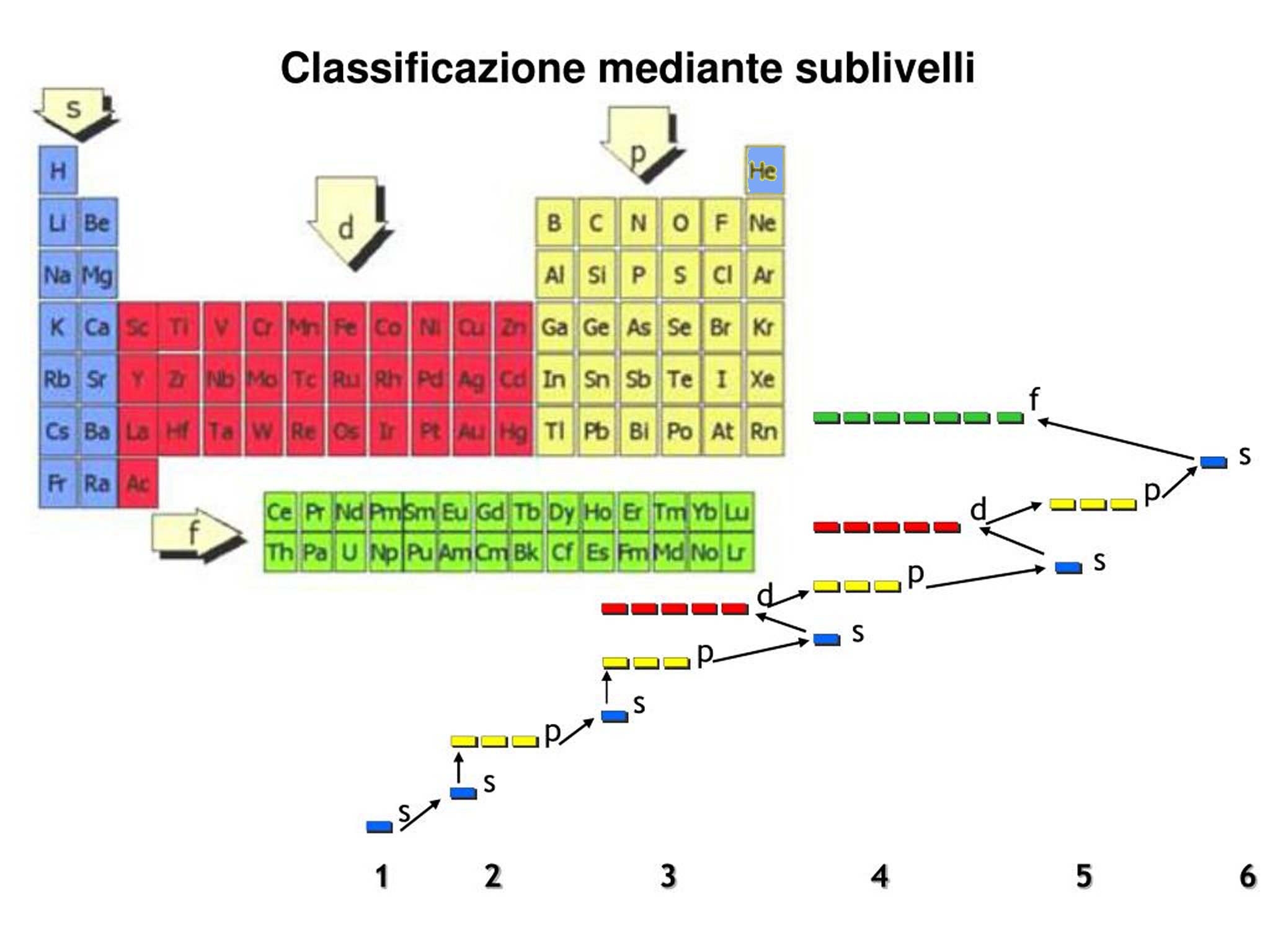
Quest'altra tabella evidenzia quale tipo di orbitale piu' esterno caratterizza ogni elemento
all'interno della Tabella Periodica. (Fa eccezione He che e' di tipo s)
livello energetico, numero e forma degli orbitali,numero di elettroni.
il livello energetico, il tipo di orbitale e quindi la sua forma, l'orientamento e l'energia associata.
dal primo dipende il secondo il secondo dal terzo, ma il quarto e' indipendente potendo avere solo due valori.
Il numero quantico principale n,
e' un numero intero che va da 1 a 7 (anche oltre ma non ha praticita' per la configurazione elettronica)Il numero quantico secondario l
indica i tipi (forme) di orbitali associati a quel livello e
indirettamente anche la loro grandezza. Dato che piu' alto e' n piu' grande e' il raggio dell'atomo
quindi n = 1 , l = 0 ... 0 = orbitale s
Riassumento:
l=0 orbitale sferico
l=1 orbitale di tipo p 2 lobi
l=2 orbitale di tipo d 4 lobi
l=3 orbitale di tipo f 8 lobi
Per l = 0 l'orbitale (s) è sferico. Al centro della sfera c'è il nucleo.


Per l = 2 = orbitale ( d ) : è a quattro lobi . Il nucleo dell'atomo sta al centro dei quattro lobi.

Per l = 3 = l'orbitale f : è a otto lobi (orbitale f).

il numero quantico magnetico ml
indica quante direzioni sono possibili per ogni orbitale nello spazio e,indirettamente il numero di orbitali possibili
infatti l=0 e' l'orbitale sferico e quindi i tre assi sono itercambiabili

ml = -1 0 1
cioe' valori di tre possibili orientamenti e quindi anche 3 orbitali

cioe' 5 possibili orientamenti e quindi 5 possibili orbitali

per l=3 ml= -3 -2 -1 0 1 2 3 ... ovvero in tutto 7 possibili orientamenti

il numero quantico di spin puo' assumere due valori -1/2 e ½
Ogni elemento
della tavola periodica ha dunque una propria precisa configurazione
elettronica
dato che a parita' dei valori di n, l, ml
il valore
di spin differenzia due atomi “similari”
Il
modo pero' in cui gli orbitali vengono occupati dagli elettoni
a
partire dall’Idrogeno sino all’Uranio e oltre sino all'elemento
118
ha una successione particolare dato
che i livelli energetici degli orbitali s p d f non sono
rigidamente in scala.
Il
loro riempimento dipende
dal fatto che che alcuni
orbitali di livello più basso
sono più energetici di
altri a livello più alto
ma
in generale lo schema di
riepimento degli orbitali e' il seguente:

ad esempio dopo il 4p viene occupato il 5s e solo successivamente il 4d

A parita di "energia" si occupano gli orbitali con un elettrone e poi si completano gli altri.
Esempio: caso degli orbitali 2p si occupa 2px poi 2py poi 2pz e solo dopo si completa il 2px
Prima pero' di passare ad un orbitale di energia superiore si completa/no quello/i di energia inferiore.








Quest'altra tabella evidenzia quale tipo di orbitale piu' esterno caratterizza ogni elemento
all'interno della Tabella Periodica. (Fa eccezione He che e' di tipo s)
